Les
Monosaccharides
- Généralités
- Caractčres
généraux
- Pas hydrolysable par des acides
faibles ŕ chaud
- On distingue deux
groupes
- Constitués uniquement de C, H,
O : monosaccharides vrais
- Constitués de C, H, O, N et
autres : dérivés de monosaccharide
- Définition
- Constitution
- CnH2nOn ou
Cn(H2O)n
- Une fonction
carbonyle
- Aldéhyde ŕ
aldose
- Cétonique ŕ
cétose
- Des fonctions alcool sur les
autres C (au moins 2)
- Exemples
- Aldose le plus simple :
glycéraldéhyde
- Cétose le plus simple :
dihydroxyacétone
- Classification
- Nombre d’atomes de carbone
- Trioses
- Tétroses
- Pentoses
- Hexoses
- Heptoses
- Nature de la fonction
carbonyle
- Aldéhydique
- Cétonique
- Formule linéaire du
glucose
- Formule
brute
- C6H12O6
- 180g/mol
- formule semi
développée
- CHO–CHOH–CHOH–CHOH–CHOH–CH2OH
- Présence de carbones asymétriques
ŕ isomčres optiques
- Formule
développée
- Obtention par synthčse d’un ose ŕ un
carbone de plus ou moins
- Synthčse de Killiani Fisher
(acide cyanhydrique HCN)
obtention de deux épimčres = oses ne différant que
par la position de la fonction –OH portée par le męme
C
- Dégradation de Wöhl
(hydroxylamine NH2OH)
- On peut alors établir la
filiation des oses
- Conséquences des
filiations
- Chaque ose peut ętre rattaché ŕ
un triose de départ
- A chaque isomčre de la série D (
-OH du dernier C ŕ droite) correspond son énantiomčre dans la
série L avec les męmes propriétés physico-chimiques (sauf
[a])
- Formules cycliques
- Objections ŕ la formule
linéaire
- Perméthylation du glucose
- Par le sulfate diméthylique
(H3C)2SO4
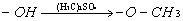
- Or expérimentalement :
fixation de 5 –CH3 au maximum, il existe donc 2 –OH
qui ne sont pas libres
- Réaction avec un alcool
- Normalement : aldéhyde +
alcool ŕ acétal
- Or on ne peut fixer qu’un
seul –OH au niveau de la fonction –CHO
- L’ose naturel est donc sous
forme cyclique, présence d’un C hémyacétalique
- Forme pyrannique des
oses
- Représentation de Tollens
- Dérivé d’un cycle
pyrannique
- Apparition d’un *C
supplémentaire
- Représentation de Haworth
- Le cycle est face au
plan
- Les 5 C et le O ne sont pas
dans le męme plan
- Forme chaise et forme
bateau
- Forme
furannique
- Dérivé d’un noyau
furannique
- Les aldohexoses se cyclisent en
forme pyrannique, les cétohexoses en forme
furannique
- Les 4 C et un O sont dans le męme
plan
- Les propriétés des
monosaccharides
- Propriétés
physiques
- Solubilité
- Trčs soluble dans
l’eau
- Si concentration trop
importante, formation de cristaux
- Peu soluble dans
l’éthanol
- Insoluble dans
l’éther
- Saveur : sucrée
- Pouvoir rotatoire [a]
- Lié ŕ la présence d’un *C,
donne l’angle de déviation (en
g-1dm-1mL)
- a (°)=
[a].C.l
- Phénomčne de mutarotation
- Deux anomčres possibles sur
le C hémiacétalyque : a et b, le phénomčne de mutarotation est
le changement progressif de l’angle de déviation de la lumičre
polarisée
- Techniques chromatographiques
- Chromatographie sur
papier
- Chromatographie sur Couche
Mince
- High Performance Liquid
Chromatography
- Chromatographie en Phase
Gaz
- Transformation en dérivé
triméthylsilylé
- Propriétés
chimiques
- Stabilité
-
| |
Milieu
acide |
Milieu
basique |
| Faible |
Stable |
Epimérisation et mutarotation accélérée |
| Fort et ŕ chaud |
Déshydratation en dérivé du furfural |
Oxydation : ils réduisent des composés minéraux et
organiques |
- Dues ŕ –COOH
- Oxydation des oses
- –C1 oxydé par I2
ou Br2 ŕ acide aldonique
- –C6 oxydé par I2
ou Br2 ŕ acide uronique
- –C1 et –C6 oxydés par
HNO3 ŕ chaud ŕ acide arique
- Oxydation par
HIO4 coupe les chaînes carbonées des
a-glycérols
- Propriétés
réductrices
- Complexes métalliques
(réactions non stoechiométriques)
- Cu2+ ŕ
méthode de Fehling et méthode de
Bertrand
- Hg2+ ŕ
méthode de Baudoin Lewin
- Fe3+ ŕ
méthode de Hagedorn Jensen
- Composés organiques
- Acide
3,5-DiNitroSalicylique (3,5-DNS)
- Réactions d’addition et de
substitution
- Action des alcools et des
phénols ŕ formation d’une liaison osidique au niveau du
carbone hémyacétalique
- Action de l’acide
cyanhydrique HCN (Killiani Fischer)
- Action d’une amine
(Wöhl)
- Action de l’acide
phosphorique (H3PO4)
- Réduction en
polyalcool
- Aldose ŕ 1 isomčre unique
(ex : glucose ŕ sorbitol)
- Cétose ŕ 2 polyalcools
épimčres (ex : fructose ŕ sorbitol + mannitol)
- Dues aux –OH
- Estérifications (action
d’acides)
- Ethérification (action
d’alcools)
- Due ŕ –OH et –COOH
- Condensation avec la
phénylhydrazine ŕ osazone
- Les oses ou monosaccharides d’origine
biologique et leurs dérivés
- Nombre de
carbones
- Trioses et tétroses
- D-Glycéraldéhyde ŕ 3
Phospho-D-Glycéraldéhyde
- DiHydroxyAcétone ŕ
PhosphoDiHydroxyAcétone
- D-Erythrose ŕ
D-Erythrose-4-Phosphate
- Pentoses
- D-Ribose (acides nucléiques,
coenzymes)
- L-Arabinose
- Hexoses
- D(+)-Glucose : trčs répandu
chez tous les organismes, libre et combiné
- D(+)-Mannose : peu abondant ŕ
l’état libre
- D(+)-Galactose : constituant
du lactose du lait, …
- D(-)-Fructose : ŕ l’état
libre et dans les osides (saccharose)
- L(-)-Sorbose : oxydation du
D-Sorbitol
- Fonctions
- Les désoxyoses = désoses
- 1 O en moins au niveau du C2
d’un aldose
- parfois en C6
- les osamines
- La fonction –OH en C2 est
remplacée par –NH2
- Trčs instable, plus courant
sous sa forme N-acétylée
- Les dérivés des osamines
N-acétylées
- Acide N-Acétyl
Muranique
- Acide neuraminique
- Cétose ŕ 9C : acide
pyruvique + D-Mannosamine ŕ A neuramin.
- Inexistant ŕ l’état libre,
se rencontre combiné ŕ acides sialiques
- Les acides uroniques
- La vitamine C : acide L-ascorbique
C6H8O6
Chapitre suivant, Chapitre Précédent
Table des matičres de ce
chapitre, Table des matičres générale