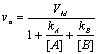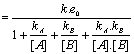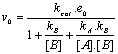- Dťfinition
- Les enzymes sont des protťines
douťes díactivitť catalytique spťcifique
- Naturellement produites
- Action hors des cellules qui les produisent
- Thermolabiles
- On dťsigne sous le nom de substrat
ce qui va Ítre transformť et produit ce qui dťcoule de la
rťaction
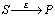
- A une rťaction correspond une seule enzyme
- En fait il existe des iso-enzymes ťlaborťes par le mÍme organisme qui catalysent la mÍme rťaction mais dont la structure protťique et certaines propriťtťs physico-chimiques sont lťgŤrement diffťrentes.
- Les enzymes sont des protťines
douťes díactivitť catalytique spťcifique
- Notion de
catalyse
- Rťaction díestťrification

hydrolyse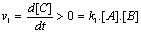
- A líťquilibre
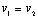
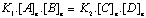
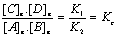
constante caractťristique de líťquilibre ŗ une tempťrature donnťe
- Modalitťs de líaction catalytique
- Rťaction díestťrification
- Moments historiques de líenzymologie
- Rťpartition des enzymes chez
les Ítres vivants
- Dans les organes et les
tissus
- Díune faÁon gťnťrale, la rťpartition des enzymes est analogue ŗ celle des substrats quíelles peuvent transformer
- Localisation dans les mÍmes organes chez les espŤces voisines
- Diffťrences immunologiques et de structure ŗ marqueurs tissulaires
- Dans la cellule
- A líintťrieur de la cellule les enzymes sont regroupťes e unitťs fonctionnelles
- Ex†: mitochondries, lysozomes
- Dans les organes et les
tissus
- Rappels
- Dťnaturation
- Passage díune structure ordonnťe ŗ une structure dťsordonnťe†: prťcipitation
- Rupture des liaisons non -
covalentes et des ponts S-S
- Pont hydrogŤne
- Liaisons hydrophobes
- Liaisons ťlectrostatiques
- La dťnaturation est
rťversible au dťpart, il existe un ťtat intermťdiaire†:
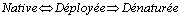
- Explications principales
- pH extrÍmes
- Solvants organiques et dťtergents
- Action du b-mercapto ťthanol
- Dťnaturation
- Structure gťnťrale des
enzymes
- Protťine monomťrique
- Rťaction directement sur la protťine
- Site actif = quelques acides aminťs
- Arrangement spatial fondamental
- Structure quaternaire†:
oligomŤres
- Autant de sites actifs que de monomŤres
- Autres ťlťments
- Cations = cofacteurs mťtalliques
- Substances organiques†: coenzymes
- Nťcessite cofacteurs + coenzyme en gťnťral
- Protťine monomťrique
- Propriťtťs gťnťrales des
coenzymes
- CaractŤres communs
- Jamais protťique
- Molťcule organique de faible masse molťculaire
- Toujours thermostable
- Non responsable de la spťcificitť
- Apparaissent dans les termes de la rťaction
- Retrouvent leur ťtat gťnťral in vivo
- SystŤmes conjuguťs (alternances des types de liaisons)
- Les deux types de coenzymes
- Dissociables†: coenzymes = transporteur
- Non dissociables†: trŤs solidement liť ŗ líapoprotťine
- CaractŤres communs
- Le site
actif
- Dťfinition
- Le site actif est une zone constituťe de quelques acides aminťs localisťs dans la zone interne hydrophobe de la protťine et au niveau de laquelle síexerce la catalyse
- Le site actif est constituť
des acides aminťs qui
- Lient les substrats ŗ site de fixation / reconnaissance
- Assurent la catalyse ŗ site catalytique
- Gťnťralitťs
- Grande diversitť
- Caractťristiques†: petits, crevasses, hydrophobe, a.a. polaires
- Arguments†: substrats petits, enzymes autocatalytiques
- Nature des groupes catalytiques du
site actif
- Seuls certains acides aminťs peuvent intervenir dans la catalyse ŗ acides aminťs polaires (His, Ser, Cys, Tyr, Lys)
- Thťories
- Ajustement induit
- Distorsion dans le substrat
- Exemples de mode díaction du site
actif
- 4 genres de
phťnomŤnes
- Positionnement de la molťcule du substrat
- Catalyse covalente†: formation díun acylenzyme (S-E)
- Catalyse gťnťrale acide - base (mvt de H+)
- Catalyse nuclťophile Ė ťlectrophile†: interactions entre charges positives partielles et charges nťgatives partielles
- Trypsine
- Ser 183, His 43, (Asp 182)
- S + E ŗ AcylE + HX
- AcylE + H2O + HY
- Chymotrypsine
- Hydrolyse ŗ droite de Phe, Trp, Tyr
- Asp 102, His 52, Ser 195, Gly 193
- Rťseau de relais de charges
- Mťtaloenzymes†: mťcanisme de catalyse covalente
- Notion de centre
catalytique
- Le centre catalytique díune enzyme est líensemble des groupements fonctionnels de líenzyme qui participent ŗ líaction catalytique
- 4 genres de
phťnomŤnes
- Dťfinition
- Spťcificitť de
rťaction
- Spťcificitť
La spťcificitť est uniquement dťterminťe par líapoenzyme- Notion díisoenzyme
- Enzymes catalysant la mÍme rťaction mais qui ont des structures lťgŤrement diffťrentes
- Combinaison de 2 monomŤres diffťrents
- Spťcificitť de
substrat
- Spťcificitť ťtroite
- Substrat
- Isomťries Z & E avec double liaison
- Isomťries optiques C*
- Produit
- Apparition de C*
- Substrat
- Spťcificitť large
- Spťcificitť de
groupe
- 1 enzyme ę 1 groupe de substances transformťes
- Ex†: b-galactosidase
- Spťcificitť basse
- Action de nombreuses substances
- Líenzyme ne reconnaÓt que la liaison†: on parle souvent de spťcificitť de liaison
- Ex†: bromťline
- Spťcificitť de
groupe
- Spťcificitť ťtroite
- Notion de complexe
activť
- Une rťaction se rťalise
- Avec une vitesse apprťciable entre deux espŤces molťculaires A et B, pour un nombre de chocs efficaces par unitť de temps suffisant
- Dans des conditions
optimales
- Orientation des molťcules
- Minimum díťnergie
- Complexe activť
- Si lors díune collision, les molťcules possŤdent G* (barriŤre ťnergťtique), elles forment une association temporaire = complexe activť et peuvent donner A + B
- La vitesse dťpend donc du nombre de complexes activťs
- Evolution de líenthalpie libre au
cours díune rťaction
- Intervention de la
potentialitť et de la vitesse
- Spontanťitť = enthalpie libre DG = G2 Ė G1
- Energie díactivation†: Ea = G* - G1
- Intervention de la
potentialitť et de la vitesse
- Une rťaction se rťalise
- RŰle des catalyseurs et des
enzymes
- G* diminue et Ea diminue pour une rťaction donnťe
- Ea diminue avec un catalyseur chimique
- Ea diminue fortement avec un catalyseur enzymatique
- Pourquoi Ea diminue avec les
enzymes
- Líenzyme offre ŗ la rťaction une voie diffťrente de la voie chimique
- Avec des enzymes, on a plusieurs ťtapes successives de Ea voisines ŗ apparition de plusieurs intermťdiaires rťactionnels. Ea global est donc la diffťrence entre S et le plus haut niveau
- Vitesse
initiale
- Gťnťralitťs
- Pendant la premiŤre pťriode†: on a un couple qui est une droite†: tangente et courbe se confondent, la pente est appelťe la vitesse initiale
- Lorsque la vitesse est constante†: ordre de rťaction 0
- Líaugmentation de líordre est due ŗ la disparition du substrat et líapparition des produits
- aA + bB ŗ P
- a et b sont les coeff. de stoechiomťtrie
- a + b†: molťcularitť = ordre global de la rťaction
- a†: ordre partiel pour A
- Les 2 ordres des rťactions
- Ordre classique
- nA ŗ nAí
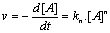 avec
n†: ordre de rťaction
avec
n†: ordre de rťaction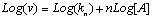
- Ordre initial
- nA ŗ níAí
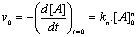
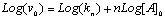
- Ordre classique
- Ordres classiques principaux
- Ordre 0†: [P] = kt
- Odre 1
- A ŗ Aí
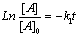 †;
†;
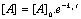
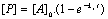
- Ordre 2
- A + B ŗ C
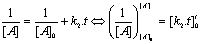
- Cas gťnťral
- Ordre 1 rťversible
- Gťnťralitťs
- Variations de
vi
- En fonction de la [enzyme]
- Les rťactions enzymatiques sont du 1er ordre par rapport ŗ la [enzyme]
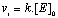
- En fonction de la [substrat]
- Pour doser des enzymes, on prťfŤre utiliser la vitesse maximum qui ne dťpend uniquement que de la concentration en enzyme
- En fonction de la [enzyme]
- Etude cinťtique de la rťaction
enzymatique
- Gťnťralitťs
- Pour expliquer la spťcificitť, on est obligť díadmettre que les enzymes forment un complexe transitoire avec le substrat, oý il y aura complťmentaritť entre le substrat et le site actif
- ŗ complexe enzyme Ė substrat spťcifique transitoire
- Equations et constantes de
Michaelis
- Simplification de líhypothŤse gťnťrale
- Constante de
Michaelis
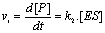
- HypothŤse de líťtat
stationnaire†:
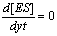
- Loi de conservation de
líenzyme†:
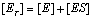
- Constante de Mickaelis†:
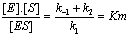
- Equation de
Mickaelis
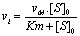
- Mťthode de King et Altman
- Equation des vitesses
intťgrťes†:
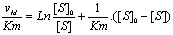
- Reprťsentation de
v0=f([S]0)
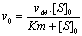
- Valeur particuliŤre†: [S]0 = Km
- Dťtermination de Km et
vM
- vi = f([S])
- Reprťsentation logarithmique†: vi = f(Log [S0])
- Reprťsentation en coordonnťes
rťciproques
- Mťthode de Limewover et
Burck†:
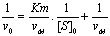
- Mťthode de Eodie-Holster†:
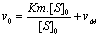
- Mťthode de Dixon / Woolf†:
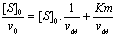
- Mťthode de Limewover et
Burck†:
- Mťthode de Eisenthal Ė
Cornish Bowden :
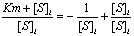
- Equation des vitesses
intťgrťes :
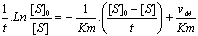
- Interprťtation de Km et de
vM
- Km :Líexpression de Km est dans certains cas beaucoup plus compliquťe que celle vue prťcťdemment
- vM
- Quand nous sommes trŤs prŤs de vM, líenzyme est saturťe, tous les sites actifs sont occupťs
- Activitť (z)
- Líactivitť est proche de vM, elle reprťsente une quantitť díenzymes qui donne cette vitesse
- Exprimťe en quantitť de substrat qui disparaÓt par unitť de temps
- En unitťs díactivitť catalytique†: qS / min
- Concentration díactivitť
catalytique
- = concentration
catalytique = catc
= activitť volumique - Exprimťe en U / L
- = concentration
catalytique = catc
- Activitť catalytique
spťcifique†: ACS
- Cíest líactivitť de líťchantillon divisťe par la masse de protťine qui permet cette activitť
- Exprimťe en U / mg†; cat / mg
- Elle reprťsente un critŤre de puretť
- Activitť catalytique
molaire†: ACM
- Cíest líactivitť catalytique de solution divisťe par la quantitť díenzymes
- = nombre de moles de substrat transformťes divisťes par unitť de temps
- Constante catalytique :
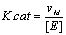
- Activitť catalytique par centre actif : = ACM / n
- Mise en ťvidence du complexe
enzyme Ė substrat
- Thťorie de líinteraction
protťine Ė ligand
- La dialyse ŗ líťquilibre permet de dťterminer Ka et le nombre n de sites pour le ligand
- Une protťine P avec n
sites rťcepteurs†:
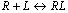
- Equation de
Scatchard†:
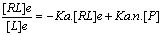
- Thťorie de líinteraction
protťine Ė ligand
- Gťnťralitťs
- Influence de la
tempťrature
- Influence de líaugmentation de la
tempťrature sur la cinťtique
- Utilisation des basses
tempťratures
- On peut refroidir brusquement un mťlange rťactionnel pour stopper une rťaction enzymatique
- Par contre, il faut ťviter un temps trop long et prťfťrer un petit volume
- Relation empirique du
Q10
- Augmentation de 10įC, v x 2 ŗ Q10 = 2
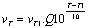
- Relation rťelle†: loi
díArrhťnius (thťorie des collisions)
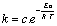
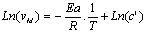
- Calcul de Ea de la rťaction
globale†:
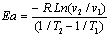
- Utilisation des basses
tempťratures
- Influence de la tempťrature sur la
dťnaturation
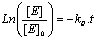
- La dťnaturation ne commence quíaprŤs q1
- La valeur de k ŗ une tempťrature donnťe va varier suivant les conditions du milieu (pH, force ionique, Ö)
- La vitesse díinactivation va síamplifier avec le degrť de purification de líenzyme et varie avec líorigine et la nature de líenzyme
- Influence de líaugmentation de la
tempťrature sur la cinťtique
- Influence du
pH
- Explications
- Action du pH sur le substrat†: il peut exister sous diffťrentes formes +/- attaquables par les enzymes
- Action du pH sur les
enzymes†:
- Sur la stabilitť conformationnelle (dťnaturation)
- Sur le site de fixation du substrat
- Sur la catalyse
- Action du pH vM et
Km
- Action du pH sur
vM†:
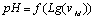
- Action du pH sur vM et Km†:
- Action du pH sur Km†: peu de variation en fonction du pH
- Le pH0 varie en fonction de líorigine de líenzyme, du substrat transformť
- Líaction du pH varie en fonction de la prťsence de substances associťes et de la durťe de la rťaction
- On dťtermine líactivitť au pH0 (tamponnť)
- Action du pH sur
vM†:
- Explications
- Les effecteurs Mickaeliens de
líactivitť enzymatique
- Gťnťralitťs
- Action primaire†: action directe de líeffecteur sur líenzyme
- Action secondaire = indirecte, líeffecteur modifie líactivitť en rťagissant avec un activateur ou un inhibiteur prťsent dans le milieu
- Effet rťversible†: líeffet disparaÓt dŤs que líeffecteur est ťliminť†: diminution de la vitesse díinhibition
- Effet irrťversible†: diminution de la vitesse díactivation
- Action des inhibiteurs
- Combinaison entre enzyme et
inhibiteur non indťpendante = association exclusive
- Inhibition compťtitive†: líenzyme fixe le substrat ou líinhibiteur, jamais les deux ŗ la fois ŗ complexes binaires ES / EI
- Gťnťralitťs†: ET = E + ES + EI
- Mťcanisme
- Cinťtique
- Pas de I†:
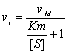
- Avec IC†:
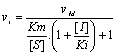
- Dťtermination de Ki
- Reprťsentation de
Dixon†:
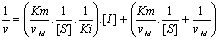
- Principaux cas díinhibition compťtitive†: excŤs de produit / substrat
- Pas de I†:
- Combinaisons entre líenzyme
et líinhibiteur indťpendantes†: associations
non-exclusives
- Inhibition non-compťtitive†:
rťcepteurs pour I et S diffťrentes ŗ complexes ternaires
ESI
- Modifications
cinťtiques
- Pas de variation de Km
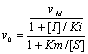
- Reprťsentation de
Dixon†:
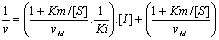
- Cas de líinhibition mixte (ŗ ťviter†!)
- Mťcanisme
- Modifications
cinťtiques
- Inhibition incompťtitive†:
rťcepteurs pour I et S diffťrents ŗ I se fixe aprŤs S,
complexes ternaires ESI
- Modifications
cinťtiques
- Diminution de vM et Km
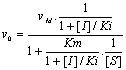
- Mťcanisme
- Modifications
cinťtiques
- Inhibition non-compťtitive†:
rťcepteurs pour I et S diffťrentes ŗ complexes ternaires
ESI
- Combinaison entre enzyme et
inhibiteur non indťpendante = association exclusive
- Action des activateurs
Mickaeliens
- Augmentation des vitesses de rťaction
- Activateurs non modifiťs
- Ions mťtalliques
- Associations
rťversibles
- Association au hasard
- Mťcanisme sťquencť
- Gťnťralitťs
- Les effecteurs
allostťriques(action sur les enzymes allostťriques non
mickaeliennes)
- Caractťristiques cinťtiques et
structurales des enzymes allostťriques
- Gťnťralitťs
- Km apparent†: vM / 2
- Coopťrativitť†: dŤs quíil y a fixation díun S, il y a modification de la structure du monomŤre qui a fixť S, cette modification se transmet aux sous-unitťs voisines qui vont fixer S plus facilement.
- Dťfinition des enzymes
allostťriques
- OligomŤres de type quaternaire, axe de symťtrie
- Effet coopťratif entre les
molťcules de S†: affinitť croissante
- Enzymes de type K†: effet coopťratif homotrope (mÍme catťgorie de S), sigmoÔde
- Enzymes de type v†: pas de coopťration, effet hťtťrotrope (entre sites diffťrents), hyperbolique
- Les deux ťtats
conformationnels
- [S] faible, ťtat dťfavorable T
- [S] ťlevť, ťtat favorable R
- Le passage de T ŗ R se fait par transition allostťrique
- Les deux thťories
- Thťorie de Koshland
- Thťorie de Monod Wyman Changeux MWC
- Les ligands vont stabiliser líenzyme dans líťtat T ou R suivant la nature du ligand
- Les deux catťgories díenzymes
allostťriques
- Type K
- v = f([S]) sigmoÔde
- Effets coopťratifs
- Km varie†; vM ne varie pas
- Reprťsentation de
Hill†:
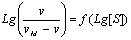
- Coeff. directeur†:
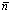 , indice de coopťrativitť
, indice de coopťrativitť - y = 0 ŗ x = Km apparent
- Coeff. directeur†:
- Type V
- VM varie, Km ne varie pas
- Disparition de la sigmoÔdicitť
- Coopťrativitťs homotropes
- Type K
- Gťnťralitťs
- Action des effecteurs
allostťriques
- Exemples
caractťristiques
- BiosynthŤse de la L-Ile ŗ partir de la Thr
- SynthŤse de nuclťotides pyrimidiques par líaspartate transcarbamylase
- Les inhibiteurs
allostťriques
- Les activateurs allostťriques
- Exemples
caractťristiques
- Action des agents de
dťsensibilisation
- La sensibilitť ŗ un effecteur allostťrique peut disparaÓtre sous líeffet díun traitement chimique (Hg / urťe / F.ion.) ou physique (congťl. / dťcongŤl.)
- La dťsensibilisation entraÓne une normalisation de la cinťtique ŗ courbe hyperbolique
- Multiplication de la coopťrativitť, suppression des interactions
- Importance des enzymes allostťriques
dans les chaÓnes de biosynthŤse
- ChaÓnes de biosynthŤse linťaire
- ChaÓnes ramifiťes
- Inhibition concertťe
- Inhibition cumulative
- Inhibition diffťrentielle
- Inhibition ťtagťe
- Caractťristiques cinťtiques et
structurales des enzymes allostťriques
- Les
coenzymes
- Rappels
- Molťcules organiques
nťcessaires ŗ líactivitť enzymatique
- Activateurs†: liťs ŗ líapoprotťine
- Transporteurs†: co-substrats
- Jamais de nature protťique
- Toujours rťgťnťrťs
- Molťcules organiques
nťcessaires ŗ líactivitť enzymatique
- Les vitamines
- Tous les coenzymes dťrivent des vitamines
- Une vitamine est une substance organique qui doit Ítre fournie dans líalimentation en trŤs petite quantitť, díune faÁon continue, pour permettre le fonctionnement de líorganisme.
- Classification
- Coenzymes des oxydorťductases
- Les nicotinamides
nuclťotides
- Vitamine impliquťe dans la
structure
- Amide nicotinique = B3 = PP
- Provitamine = acide nicotinique
- B3 ŗ NAD+ / NADP+
- La structure du NAD+
- Les propriťtťs
- Absorbance max†: l = 260, 340 nm
- Fluorescence (ťmission ŗ 460 nm)
- Travail en milieu tamponnť pour la stabilitť
- Rťactions díoxydorťduction
- Vitamine impliquťe dans la
structure
- Les flavines
nuclťotides
- Vitamine impliquťe dans la
structure
- B2 = riboflavine = lactoflavine
- = colorant E101 (jaune)
- trŤs sensible ŗ la lumiŤre
- Les coenzymes qui dťrivent
de la vitamine B2
- FMN†: Flavine MonoNuclťotide
- FAD†: Flavine Adťnine Dinuclťotide
- Mťcanismes díaction
- Coenzymes trŤs fortement liťs ŗ la protťine = flavoprotťine
- Deux formes semi-quinoniques
- Vitamine impliquťe dans la
structure
- Les coenzymes
hťmatiniques
- Fortement liťs aux protťines
- Structure tťtrapyrolyque centrťe sur un atome de Fe2+
- Fonction†: CytFe3+ ů CytFe2+
- Autres enzymes
díoxydorťduction
- Acide lipoÔque
- ŗ intervention dans les dťcarboxylations
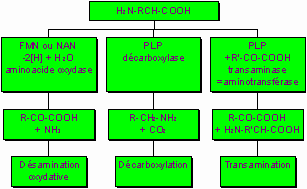
- Les nicotinamides
nuclťotides
- Les coenzymes de transfert de
groupement
† Pyridoxal-Phosphate (PLP†; PALP) Thiamine PyroPhosphate (TPP+†; DPT+) Coenzyme A Coenzymes du mťtabolisme des radicaux monocarbonťs Vitamine Vitamine B6 = pyridoxine (hydrosoluble) Vitamine B1 = thiamine Vitamine B5 = acide panthatťnique Acide folique = B9 ŗ Acide Tťtra HydroPholiq. Vit. B12 ŗ CoEnz B12
Adťnosyl Mťthionine (-CH3)
Vit. B8 ŗ Biotine
Coenzyme PLP ( 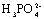 -B6)
-B6)TPP+ (Thiam.- 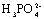 )
)CoA-SH Mťcanisme Transamination des AA
Dťcarboxylation des AA
Clivage des AA
EliminationSystŤme ping-pong avec nbx liaisons (ioniques, hydrogŤne hydrophobes)
Dťcarboxylation oxydative des Aacťto Dťcarboxylation simple des Aacťto
-SH se fixe aux ĖCOOH ŗ acylcoezyme A R-CO~SCoA
- Rappels
- Cinťtique michaťlienne ŗ deux
substrats
- A + B ů P + Q (intervention díun coenzyme transporteur). Si B = H2O†; on ramŤne ŗ 1 seul substrat. Il existe des mťcanismes * complexe ternaire (EAB). et des complexe binaire (EA ou EB). On parle de * systŤme sťquentiel (SS Ė PP). * systŤme non sťquentiel (S Ė P Ė S Ė P®)
- SystŤme ŗ complexe binaire
(bi-bi)
- SystŤme ping pong
- Non sťquencť†; ordonnť
- Rťaction ŗ double dťplacement
- Un seul site de fixation pour le substrat
- Cinťtique
- Mťcanisme de Theroell et
Chance
- E + A ů EA || EA + B ů E + P + Q
- SystŤme ping pong
- Cinťtique ŗ complexe ternaire
- Mťcanismes díassociation
alťatoire substrat Ė enzyme (bi-bi alťatoire)
- Cas gťnťral†: associations
de A et de B avec E dťpendantes
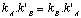
- Reprťsentation de Cleland
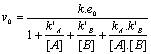
- Reprťsentation
secondaire†:
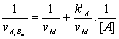
- Cas simplifiť†: association
indťpendante ŗ KA et KB
- Reprťsentation de
Cleland
- Reprťsentation
secondaire†:
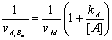
- Reprťsentation de
Cleland
- Cas gťnťral†: associations
de A et de B avec E dťpendantes
- Mťcanisme ordonnť (bi-bi
ordonnť)
- E + A ů EA ů EAB ŗ E +P + Q
- Reprťsentation de
Cleland
- Equation des
vitesses
- Dťtermination des
constantes†:
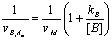
- Equation des
vitesses
- Dťtermination du
mťcanisme rťactionnel
- Graphiquement†:
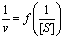
- Inhibiteurs par excŤs de produit
-
Mťcanismes
Produits
Substrat variable
†
†
Ordonnť bi-bi
Theorell / Chance bi-bi
Ping-pong bi-bi
†
Alťatoire bi-bi
†
†
P
QP
QP
QP ou Q
A
B
B non - saturant
B saturant
A non - saturant
A saturant
NC
CNC
CNC
CC
IC
C-
C-
C-
NC
NCC
NCC
NCC
NC
-C
-C
--
- DíaprŤs líaction des
analogues structuraux
- Bí IC de E pour B, A cst, Bí analogue structural de B
- B fixe, A
variable en prťsence de Bí ŗ mťcanisme alťatoire ŗ
complexe ternaire (INC de E pour A, B fixe)
un site pour S, un site pour I - Ou ŗ mťcanisme
ordonnť ŗ complexe ternaire (II pour A, B
fixe)
un site pour A, un site pour Bí = site de B
- Graphiquement†:
- Remarque†: rťversibilitť des rťactions enzymatiques (Rťaction de Maldane, cinťtiques ŗ deux substrats)
- Mťcanismes díassociation
alťatoire substrat Ė enzyme (bi-bi alťatoire)